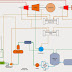
Korosi adalah kembalinya logam ke bentuk
bijihnya, karena logam sebenarnya tidak stabil. Berikut kutipan dari Schweitzer, P.A (2010):
Pengecualian proses korosi terjadi pada logam emas/gold (Au) dan platinum (Pt) karena sudah berada pada keadaan dasar yang stabil.
Proses bijih menjadi logam
dibuat dengan temperatur yang tinggi sehingga menghasilkan keadaan logam yang
berenergi tinggi dan jika aliran arus energi tidak ada (selama logam dipakai)
maka logam akan cenderung kembali ke bentuk bijihnya sehingga semakin lama
logam terkikis habis dan inilah terjadinya Proses Korosi.
Secara reaksi kimia, proses korosi terjadi karena
potensial reduksi (ERed) besi
lebih rendah daripada ERed
di sekelilingnya (udara dan air), sesuai reaksi :
Anoda (-) : 2 Fe ---> 2 Fe2+ + 4e
Katoda (+) : O2 + 2 H2O + 4e
---> 4 OH-
Sehingga reaksi menjadi :
2 Fe + O2 + 2 H2O
---> 2 Fe2+ + 4 OH-
2 Fe + O2 + 2 H2O ---> 2 Fe(OH)2
4
Fe(OH)2 + 2 H2O + O2 ---> 4 Fe(OH)3
(korosi)
"Corrosion
is the return metal into ore, because the metal is actually unstable. Process
ore to be a metal made by high temperature so produce high energy metal and if
no current flow (during metal used) so metal will tend return into ore so longer
time the metal is eroded and this is Corrotion Process.
In
chemical reaction, corrosion process occur due to potential reduction iron
lower than environment potential reduction (air and water), according reaction
:"
DERET VOLTA :
(LiKaBaCaNaManganAluZengBesiNibaniSangPrabuHanCurHangusAgakPaitAu)
- Dari Kiri ke Kanan nilai ERed (potensial reduksi) semakin positif (+), Mengalami Reduksi (Oksidator Kuat)
- Dari Kanan ke Kiri nilai ERed semakin negatif (-), mengalami Oksidasi (Reduktor Kuat)
Sel Volta / Sel Galvani berkebalikan dengan Sel Elektrolisis.
Ciri - Ciri Sel Volta Seperti Dibawah Ini :
- Katoda (+) : Fe ---> Fe2+ + 2e mengalami Reduksi
- Anoda (-) : Mg2+ + 2e ---> Mg mengalami Oksidasi
BACA JUGA: Sel Elektrokimia : SEl VOLTA / SEL GALVANI (1 of 2)
Macam - Macam Perlindungan Logam Terhadap Korosi:
Macam - Macam Perlindungan Logam Terhadap Korosi:
1. Perlindungan
Katoda (Cathodic Protection) adalah upaya mengurangi perbedaan
potensial reduksi antara 2 logam (katoda dan anoda), terbagi menjadi 2 jenis
yaitu :
- Pengorbanan Anoda (Sacrificial Anode)
Logam yang akan dilindungi bertindak sebagai Katoda
(reduksi) karena logam pelindung yang akan korosi lebih dahulu dicarikan yang
mempunyai ERed rendah
yang ditempatkan sebagai Anoda (oksidasi). Karena reaksi korosi terjadi akibat
reaksi oksidasi dan reaksi oksidasi terjadi di Anoda maka yang akan terkikis
adalah Anoda saja dan Katoda terlindungi sehingga disebut Pengorbanan Anoda dan
antara keduanya dihubungkan kawat penghantar untuk perpindahan elektron.
Prinsip kerjanya sama dengan proses Sel
Volta yaitu larutan elektrolit yang tercelup di 2 elektrode,
karena ada beda potensial antara kedua elektrode maka ada elektrode yang
menerima elektron (reduksi) dan melepas elektron (oksidasi).
Prinsip pemilihan Anoda mengacu ke Deret Volta yaitu logam pelindung harus di
sebelah kiri dari logam yang dilindungi. Misalnya tiang listrik yang terpendam
di tanah lembab (elektrolit)
terbuat dari besi (katoda), maka logam pelindungnya harus
disebelah kiri Fe yaitu Mg, Al atau Zn. Sebagai contoh Mg (anoda)
akan teroksidasi lebih dahulu sehingga Fe akan aman dari pengkorosian dini.
Reaksinya seperti berikut :
"The
metal to be protected acts as a cathode (reduction) because metal protector
will first corrosion choosen has low potential reduction and have placed as
anode (oxidation). Because corrosion react occur oxidation react and occur in
anode, so it will be eroded only anode and cathode will protected so called sacrificial
anode and both connected by connected wire for electron transport. The working
principle like process in volta cell which electrolyte solution dipped in 2
electrode, because there is potential different between two electrode so there
is electrode accept electron (reduction) and donor electron (oxidation). The
principle select of anode refers to volta sequence which protect metal must in
left from protected metal. As example electric tower that dipped in humid soil
(electrolite) made from iron (cathode), so protection metal must in the left
from iron such as Mg, Al or Zn. As example Mg (anode) will be oxidated first so
iron will save from corrosion. Reaction like below :"
Anoda (+): Mg ---> Mg2+ + 2e
Di sekitar Katoda (-) : H2O + 2e
---> H2 + 2 OH-
Sehingga reaksi menjadi: Mg + H2O --->
Mg2+ + 2 OH- + H2
Mg + H2O ---> Mg(OH)2 + H2
Sumber: Chapter 19 The Book principles of General
Chemistry "Electrochemistry"
- Arus Terpasang (Impressed Current)
Prinsipnya mirip Sel
Elektrolisis yaitu menggunakan Arus DC (jika menggunakan arus AC harus ada Rectifier sebagai penyearah arus) dan Katoda Inert yang tidak habis terkikis. Arus DC digunakan untuk mensupplay arus
negatif (-) ke logam yang dilindungi sebagai Katoda (-) dan arus positif (+) ke Anoda (Pt) karena Inert tidak ada reaksi oksidasi. Arus listrik mengalir dari Anoda (+)
ke Katoda (-) sehingga aliran elektron berkebalikan yaitu
dari Katoda (-) ke Anoda (+), dengan adanya penambahan elektron di Anoda
menyebabkan Anoda yang semula melepas elektron berubah menjadi penerima
elektron yaitu dipaksa bertindak menjadi Katoda sehingga reaksi oksidasi tidak
terjadi. Elektron yang dihasilkan dari arus disyaratkan menghasilkan elektron
lebih tinggi dari hasil reaksi di Anoda sehingga menyebabkan Anode kelebihan
elektron.
"The
principle is similar electrolysis cells using DC current (if use AC current
must use Rectifier) and Inert Cothode which not react will be eroded. DC
current used to supply negative current (-) to protected metal as Cathode (-)
and positive current (+) to Anode (Pt) because Inert does not oxidation react.
Electric current distribute from Anode (+) to Cathode (-) so electron flow
reverse such as from Cathode (-) to Anode (+) with adding electron in Anode
causing Anode that firstly release electron change to acceptor electron which
forced acts as Cathode so oxidation react does not occur. Electron that
produced from it's current must be required produce electron higher than
reaction in Anode so cause an excess electron Anode."
2. Penyepuhan
(ElectroPlating)
Menggunakan
prinsip Elektrolisis dengan pelapisan logam menggunakan logam mulia (Sn, Zn,
Cr, Ni, Au, Ag). Contoh umum adalah :
- Kaleng terbuat dari besi (Fe) menggunakan plating dari Timah (Sn), sehingga kaleng terlindungi dari pengkorosian selama lapisan Timah tidak tergores dan jika tergores (kaleng sudah dipakai), Timah akan mengkorosi Besi karena ERed Timah terletak disebelah kanan Besi (Besi lebih oksidatif dari Timah) sehingga proses penghancuran limbah juga menjadi cepat (limbah hancur lebih cepat dan ini diharapkan).
- Proses pelapisan logam dengan Cu
- "The bottles are manufactured from Iron (Fe) using plating from Tin (Sn), so the botlles are protected from corrosion during Tin layer does not scratched (the bottles have been used), Tin will corrode Iron because potential reduction Tin located on the right side from Iron (Iron is more oxidative from Tin) so waste destruction process become faster (this is expected)
- Metal coating process with Cu"
3. Paduan Logam
(Alloy)
Melapisi logam dengan logam tahan karat seperti
Chromium (Cr), Nikel (Ni), Timah (Sn). Contoh alloy adalah : Kuningan,
Perunggu, Stainless Steel, Monel
Melapisi logam dengan cat, plastik atau oli sehingga
agen penyebab korosi (oksigen, pH asam, pH basa, dan kelembaban) tidak kontak
dengan logam. Tipe - tipe pelapisan adalah :
- Pelapisan dengan Penempelan (Clad Coating)
Melapisi logam dengan plastik
- Pencelupan Panas dengan Timah (Hot Dipping Tin Plating)
Pelapisan logam dengan cara dicelupkan ke lelehan timah
panas
- Galvanisasi
Pelapisan logam dengan logam lain, misalnya logam Fe
dilapisi dengan lelehan Zn (pemilihan logam pelapis mengacu ke Deret Volta
sehingga mengikuti Reaksi Galvani)
- Penyemprotan (Spraying)
Pelapisan logam dengan cara disemprot menggunakan
spray gun yang berisi lelehan panas Al atau Zn
- Pembentukan Lapisan Oksida (Passivation)
Pembentukan lapisan oksida bisa didapatkan dengan cara
pemanasan pada suhu tinggi, oksidasi kimia antara Steel dengan Hot Alkaline Nitrate / Persulphate / Perchlorat, oksidasi Anoda dengan prinsip elektrolisis.
"The
forming oxide layer can be obtained with high temperature heating,chemical
oxidation between Steel with Hot
Alkaline Nitrate / Persulphate / Perchlorat, Anode oxidation with electrolysis
principle."
- Phospatting
Pelapisan
Besi menggunakan Iron Phospate (Fe3(PO4)2 dengan
cara pencelupan di larutan H3PO4 dan ZnPO4.
Logam yang terlapisi ini masih kurang aman terhadap korosi karena permukaan
masih berpori sehingga perlu dilapisi lagi dengan pengecatan (paint). Aplikasi
ini terbanyak diterapkan di dunia otomotif.
"Coating
Iron using Iron Phospate (Fe3(PO4)2 with
dipping in H3PO4 and ZnPO4 solutions. The coated metal
still saveless to corrosion because it's surface still has porous so require
again with painting. This application many apllied in otomotive company."
6. Menghilangkan
Agen Pengoksida Logam (Reduktor Kuat)
7. Menghambat
Reaksi Kimia di Permukaan (Chemical Inhibitor & pH Control)
Mekanisme
dari chemical inhibitor adalah:
- Menyerap ke permukaan logam untuk membentuk lapisan pelindung
- Bergabung dengan produk penyebab korosi untuk membentuk lapisan pelindung logam
- Membentuk lapisan endapan seperti Coating dan melindungi lapisan logam
- "Absorb into metal surface to form a protective layer
- Join with product corrosion agent to make metal protective layer
- To form sediment layer such as Coating and protec metal layer"
Kutip Artikel ini Sebagai Referensi (Citation):
Feriyanto, Y.E. (2015). Macam - Macam Cara Pencegahan Korosi. www.caesarvery.com. Surabaya
Referensi:
[1]
http://www.npl.co.uk/upload/pdf/cathodic_protection_in_practise
[2]
http://www.corrosionsource.com/FreeContent/1/Cathodic+Protection
[3]http://chemwiki.ucdavis.edu/Analytical_Chemistry/Electrochemistry/Case_Studies/Corrosion
[4]
http://www.npl.co.uk/upload/pdf/cathodic_protection.pdf/Sacrificial_Anode
[5]http://tinker-rasor.com/wp-content/uploads/2013/03/Cathodic-Protection-Manual
[6]
http://www.bushman.cc/pdf/corrosion_theory
[7]
http://www.northeastgas.org/pdf/d_rossi_cathodic
[8]
http://www.cathodic.co.uk/files/1246442149Cathodic%20Protection%20Overview
[9] Drs. Suhartana, MSi. Laboratorium Kimia Anorganik
Fakultas MIPA Universitas Diponegoro
[10]
http://nzic.org.nz/ChemProcesses/metals/8J
[11]
http://user.engineering.uiowa.edu/~swan/courses/53086/Corrosion_Protection
[12]http://www.kau.edu.sa/Files/0060757/Subject/CORROSION%20CONTROL%
20ChE%20311
20ChE%20311
[13] Schweitzer, P.A. (2010). Handbook of Fundamentals of Corrosion Mechanisms, Causes, and Preventative Methods. CRC Press. London & New York
ARTIKEL TERKAIT:
1. Design Cathodic Protection di Condensor
2. Analisa Kerak Tube Boiler & Condenser
3. Water Process dan Injeksi Kimia di PLTU
ARTIKEL TERKAIT:
1. Design Cathodic Protection di Condensor
2. Analisa Kerak Tube Boiler & Condenser
3. Water Process dan Injeksi Kimia di PLTU
Previous
« Prev Post
« Prev Post
Next
Next Post »
Next Post »